

发布时间:2026-03-30
近日,中国科学院脑科学与智能技术卓越创新中心(神经科学研究所)孙衍刚研究组在Neuron在线发表题为《Alteration of cellular representation in the central amygdala mediates stress-induced analgesia in mice》的研究论文,该研究系统解析了急性应激如何通过中央杏仁核中特定神经元亚型及其局部环路调控疼痛,为理解情绪与疼痛之间的相互作用提供了新的视角。
在日常生活中,我们可能都有类似的体验:在突发危险的时刻,即使是受伤,当下往往并不会立刻感到疼痛,反而是在情绪平复后,疼痛才逐渐显现。这种看似“迟钝”的反应,其实是大脑的一种精妙调控机制,被称为“应激诱导镇痛”(Stress-induced analgesia, SIA)。也就是说,在急性应激状态下,大脑会主动“压低”疼痛信号,让机体暂时忽略伤痛。从进化的角度来看,这种机制具有重要意义:当个体面临危险时,最关键的任务是迅速逃离或进行防御,而不是被疼痛分散注意力。换句话说,大脑在关键时刻会重新排序各种信息的“优先级”,将生存相关的行为置于首位。那么,大脑究竟是如何实现这一调控的?哪些神经元在其中发挥关键作用?不同类型的神经细胞又是如何协同,完成对疼痛的“精准抑制”?这些问题都值得探究。尽管已有研究提示,多种神经调控系统参与其中,但在细胞类型和具体神经环路层面的机制,仍有待研究。
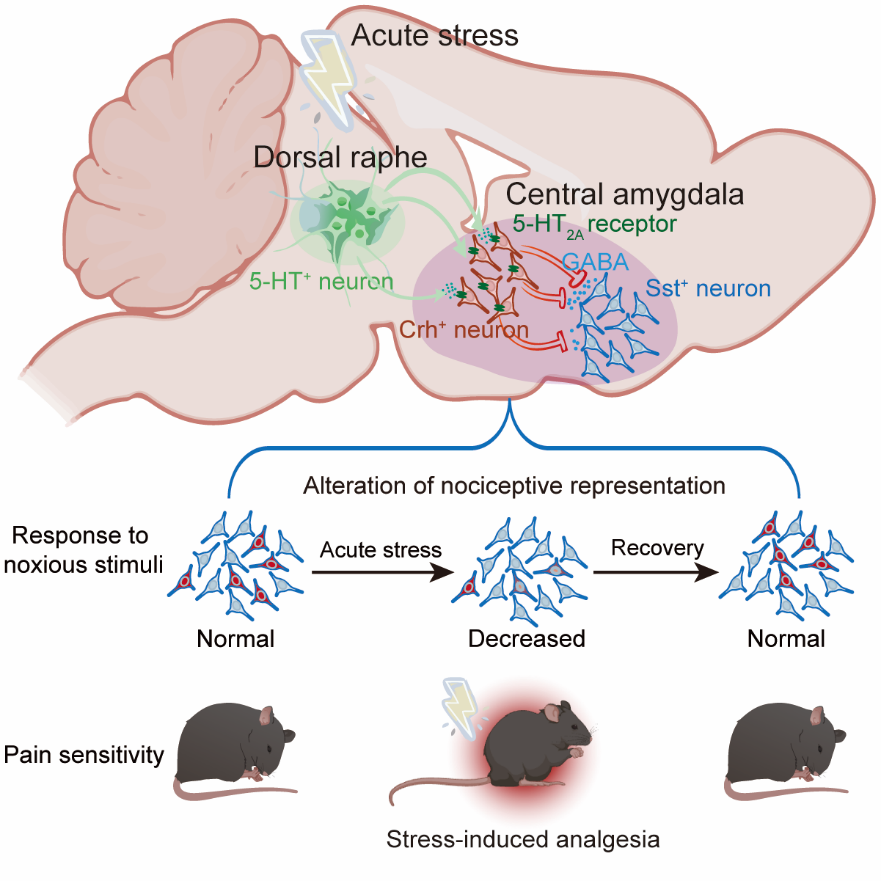
图1 中央杏仁核介导急性应激镇痛的神经机制。
中央杏仁核(central amygdala, CeA)是情绪与疼痛加工的重要脑区,主要由三类抑制性神经元构成:Sst⁺、Crh⁺和Pkc-δ⁺神经元。研究团队利用在体钙成像技术,系统分析了不同神经元亚型对伤害性刺激的表征模式,发现Sst⁺神经元中的一个亚群对伤害性刺激(如热痛和机械痛)具有显著的选择性响应。Sst⁺神经元存在一个选择性表征伤害性刺激的亚群,这说明中央杏仁核中存在参与痛觉表征的神经元群体。
进一步研究表明,在急性应激状态下,CeA中Sst⁺神经元对疼痛刺激的响应显著下降。这种抑制具有明显的选择性,也就是说急性应激并非对所有感觉输入进行普遍抑制。在应激状态解除后,Sst⁺神经元神经活动能够恢复至基线水平,提示急性应激对疼痛信号的调控具有可逆性与状态依赖性。这一结果表明,大脑在应激状态下并非整体降低感知能力,而是选择性地削弱对疼痛信息的处理。
那么,究竟是什么机制“关闭”了这些疼痛信号?研究发现,在应激过程中,Crh⁺神经元被优先激活,并通过局部GABA能抑制环路直接抑制Sst⁺神经元的活动。通过化学遗传学和光遗传学手段抑制Crh⁺神经元,可显著削弱应激诱导的镇痛效应,表明Crh⁺神经元是调控该过程的关键节点。
进一步的环路研究表明中缝背核(dorsal raphe nucleus, DRN)中的神经元在应激过程中持续被激活,并通过投射至中央杏仁核,作用于Crh⁺神经元上的5-HT2A受体,从而触发镇痛效应。敲低Crh⁺神经元中的5-HT2A受体可显著阻断应激诱导的镇痛效应,进一步验证了该信号通路在该过程中的关键作用。
综上,该研究系统揭示了中央杏仁核中不同神经元亚群在应激状态下如何通过局部抑制性环路,实现“状态依赖”的疼痛调控机制。这一发现不仅深化了对应激镇痛神经基础的认识,也为未来开发针对情绪相关疼痛障碍(如焦虑或抑郁伴随的慢性疼痛)的干预策略提供了潜在的靶点。
脑智卓越中心孙衍刚研究员为本论文通讯作者,博士研究生王林翰为本论文第一作者。脑智卓越中心韩怡斐、周婉秋、李清、刘媛以及上海交通大学瑞金医院孟莹做出了重要贡献。该研究得到了国家科技部、基金委、脑认知与类脑智能全国重点实验室以及新基石科学基金会的资助。
 附件下载:
附件下载: 